哺乳动物的卵母细胞在胚胎期形成以后,就停止了DNA复制,进入长达几十年的细胞周期阻滞。而受精是个体生命的起点,受精以后短时间内雌雄原核中的DNA重新启动复制,并且伴随着剧烈的基因组重编程和表观遗传修饰的改变。因此,受精卵的第一次细胞分裂与体细胞的普通细胞周期相比,具有非常多的独特之处。很多分子参与受精卵细胞周期进程的调控,从而开启新生命的发育程序。
浙江大学教授范衡宇实验室研究发现,CRL4泛素连接酶的一个底物识别蛋白Dcaf2(DDB1-cullin 4- associated factor-2,也叫CDT2或DTL)在小鼠卵母细胞和受精卵中高表达。Dcaf2在体外培养细胞系中的已知功能是在DNA复制过程中抑制重复复制、维持基因组稳定,但是Dcaf2在体内生长发育的哺乳动物细胞中具有怎样的生理功能目前还没有研究。特别是,Dcaf2基因敲除小鼠胚胎在8细胞期即死亡,因此阻碍了人们详细研究Dcaf2在体内细胞发育过程中的功能。
本研究制作了Dcaf2 LoxP小鼠,并与Gdf9-Cre工具小鼠杂交,得到了卵母细胞特异性Dcaf2条件基因敲除小鼠。与体细胞不同,敲除Dcaf2对卵母细胞的存活、生长和减数分裂细胞周期进程并没有影响。但是,这些缺失母源性Dcaf2的卵母细胞受精以后,虽然能够形成雌雄原核,但不能发生卵裂,阻滞在1细胞期,从而造成雌性完全不育。进一步研究发现,母源性Dcaf2敲除以后,造成DNA复制启始因子CDT1过度积累,受精卵可以启动但是不能终止第一次基因组复制,从而使受精卵积累了大量DNA损伤,无法完成细胞周期的G2/M转换。另外,这种基因组不稳定性也造成了表观遗传修饰,比如DNA五羟甲基化的紊乱,影响了受精卵基因组重构。
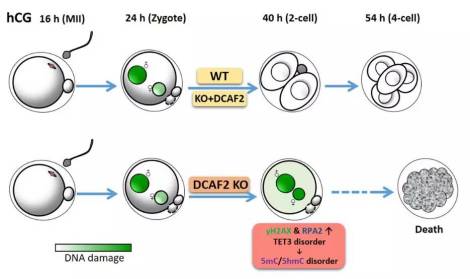
图:母源性Dcaf2在受精卵基因组稳定性维持中的功能示意图
本研究首次证明Dcaf2是保障受精卵第一次DNA复制顺利完成的母源性因子,也首次研究了Dcaf2在哺乳动物体内特定细胞类型(卵母细胞)中的生理功能,进一步阐明了CRL4泛素连接酶维持正常雌性生殖过程的分子机制。
参考文献:Maternal DCAF2 is Crucial for Maintenance of Genome Stability during the First Cell Cycle in Mice,JCS Advance Online Article,Posted on 17 August 2017
本文由博雅基因翻译作品,未经允许,不可转载。













